Die Osteograft Produktwelt
In Deutschland sind allogene Zell- und Gewebetransplantate als Arzneimittel reguliert und zulassungspflichtig, das heißt die Herstellung, die biologische Sicherheit und die klinische Anwendung unterliegen der ständigen Kontrolle der deutschen Behörden. Das DIZG verfügt über 10 Arzneimittelzulassungen für humane Gewebetransplantate.
Allogene Transplantate
Das System zur Gewährleistung der biologischen Sicherheit der Gewebetransplantate des DIZG besteht aus umfangreichen Kriterien zur Spenderauswahl, einem umfassenden, die Anforderungen der EU-Richtlinie 23/2004 weit übersteigenden serologischen Spenderscreening, das 4 Virus-Genom-Untersuchungen einschließt, der Anwendung eines validierten Verfahrens zur Entfernung/Inaktivierung von Viren, Bakterien und Pilzen und In-Prozess- und Endkontrollen am Transplantat.
Das DIZG und die ARGON sind nach DIN EN ISO 13485 zertiziert und folgen dem Ethical Code und den Qualitätsstandards der European Association of Tissue Banks (EATB).
Die Anwendung der Transplantate des DIZG ist gemäß Transplantationsgesetz (TPG) dokumentationspflichtig.
Dafür sind jeder Packung Etiketten für die Patientenakte beigefügt.
Alle Abmessungen sind Zirka- und Mindestangaben. Sie unterliegen einer präparations- und gewebebedingten Streuung. Erklärungen und Hinweise zur Applikation der Transplantate sind den jeder Verpackung beigefügten Gebrauchs- und Fachinformationen zu entnehmen.

Das gemeinnützige DIZG – Deutsches Institut für Zell- und Gewebeersatz

Anwendungen/Indikation
Quickfinder Produkte:
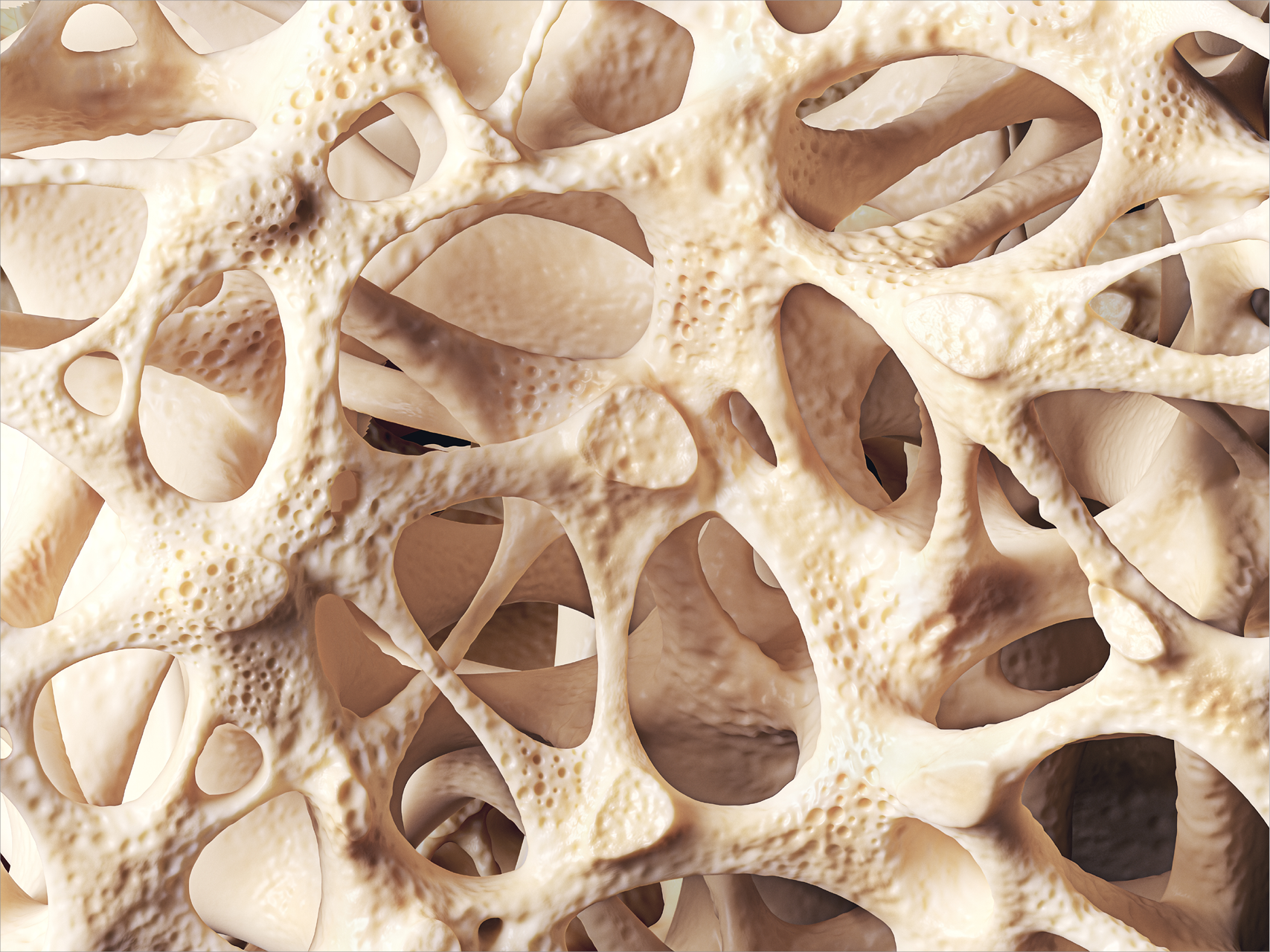
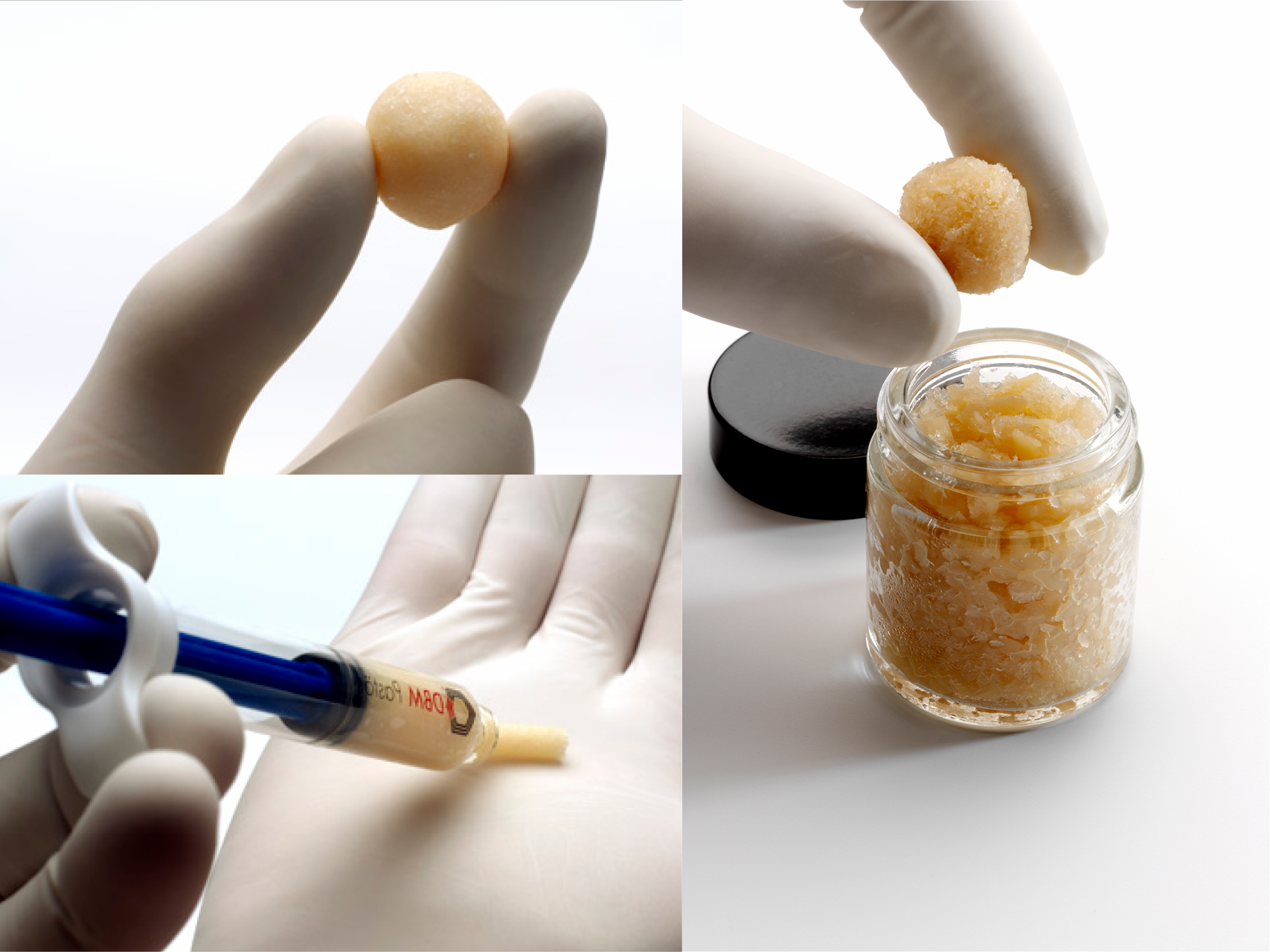
Demineralisierte Knochenmatrix (DBM) pastös
Demineralisierte Knochenmatrix (DBM) in pastöser Form ist wegweisend für Augmentation. Sie fördert Knochenwachstum und Heilung, verbessert die Knochenqualität und optimiert chirurgische Ergebnisse.
Osteogel
Hochpräzise, modulare Systeme, die nach Ihren Wünschen und den von Ihnen verwendeten Gewindedesigns und -Längen individuell zusammengestellt werden können, aber an einem Ort!